为提高研究者发起类临床研究的质量,更好的服务于临床研究工作者,按照《中山大学中山眼科中心研究者发起类临床研究项目管理办法(试行)》,临床研究中心从即日起优化项目立项管理流程,操作过程如下:
一、登录OA系统,在“流程中心”>>“临床研究中心”>>“研究者发起类临床研究项目立项流程-1”填写立项申请,并按要求上传下列附件:
1、研究方案(可参考OA“文档管理”>>“临床研究中心”的模板)
2、知情同意书
3、主要研究者简历、最高学历证书、执业资格证书扫描件
二、临床研究中心办公室形式审核后,生成“临床研究项目受理号”并于OA流程上作出回复。
三、项目负责人凭“临床研究项目受理号”,向中心医学伦理委员会申请伦理审查。
四、项目通过伦理审查后,再次登录OA,填写“研究者发起类临床研究项目立项流程-2”,并按要求上传下列附件:
1、研究方案、知情同意书、病例报告表、伦理批件
2、人类遗传资源审批决定书或备案证明、项目合同、境外资助批件等(如涉及)
五、临床研究中心办公室完成流程审批,生成“临床研究项目立项批件”并给予项目组。
六、项目组在启动前将相关资料交予临床研究中心办公室存档(一式两份),设立项目管理文件夹,完成立项。
注意事项:
1、项目如涉及人类遗传资源、境外资助、合同签署等审批工作,需按中心相关规定执行。
2、所有临床研究项目必须在获得“临床研究项目立项批件”,且在临床研究中心设立管理文件夹后方能启动。
3、获得伦理批件后,入组第一例受试者前,建议研究者对项目进行网上注册,以下注册网站供参考:
(1)中国临床试验注册中心,网址http://www.chictr.org.cn/index.aspx
(2)美国临床试验数据库,网址https://clinicaltrials.gov/
4、研究者发起类临床研究项目管理流程(见下图)
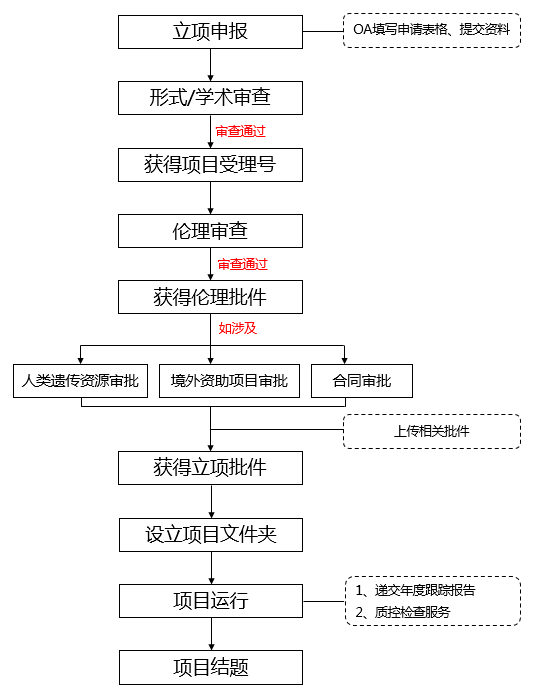
5、项目涉及的诊疗费用报销的,禁止使用医保结算临床研究相关费用,例如发票上不能出现医保字样。
如有疑问和需要协助,欢迎咨询我们:
1、临床研究中心办公室: 陈老师,电话:020-66610720(临床楼1105室)
2、医学伦理委员会办公室:颜老师,电话:18924106928(临床楼1114室)
临床研究中心
2020年8月17日