
文献链接:https://jamanetwork.com/journals/jama/fullarticle/2732608
背景介绍
玻璃体内腔内注射抗VEGF药物已成为治疗糖尿病黄斑水肿的一线临床治疗方法,尤其是对于累及黄斑中心凹(CI-DME)且视力损害的患者(视力≤20/32)。但是对于视力较好(≥20/25)的患者,治疗与否及如何治疗仍存在争议。
针对上述问题,该研究采用RCT设计,比较了对于视力较好的CI-DME首诊患者,阿柏西普玻璃体腔注射、激光和随访三种方法的效果,本期文献解读系列拟以上述研究为例,对“随机对照临床试验”的方法进行解读。
一、 随机对照临床试验的伦理:
临床试验应优先考虑到人的利益及相关的伦理道德问题,必须符合《赫尔辛基宣言》和国际医学科学组织委员会颁布的《人体生物医学研究国际道德指南》,开展试验必须获得所在医疗单位或有关部门伦理委员会的批准,同时得到受试对象或其家属、监护人的知情同意。
二、 随机对照临床试验的注册登记
临床试验开展前应首先进行临床试验注册
伦理学方面:保障“临床试验相关各”的知情权,确保试验符合伦理要求;有利于知识共享,符合公众利益。
科学合理性方面:确保研究过程的透明,可以保障研究质量,增加结果可信度,此外,可以减少重复研究,减少发表偏倚;目前有许多可供选择的注册中心
美国国立卫生研究院的临床试验网站http://www.clinicaltrials.gov
中国临床试验注册中心http://www.chictr.org
三、随机对照临床试验“方法”部分的要素
临床研究的报告应遵循临床试验报告的统一标准(Consolidated standards of reporting trials,CONSORT),该标准第一版发表于1996年,2001年进行第一次修订,目前通用的版本为2010年的第二次修订版,最早采用该标准的有JAMA、NEJM、 BMJ、LANCET和ANN INTERN MED(内科学年鉴)等,应用该标准的实践结果表明,该标准有助于医务人员了解试验背景、原理、目的、研究人群、干预措施、随机方法、统计分析,有助于相关医务人员对试验的科学性和严谨性进行评估,有助于研究者提高临床研究设计水平。CONSORT中关于研究方法为第3-12条,具体条目如下:
试验设计
3a描述试验设计 (诸如平行、析因) 包括人数分配比例
3b对研究开始后方法上的重要改变进行解释,比如试验开始后纳入标准的改变

受试者
4a受试者的纳入、排除和退出标准
4b数据收集的环境及地点
4c伦理学至上原则


干预方法
5详述每组干预的细节(以便其它研究者的复制)及实际实施情况,包括了实施时间和实施方式


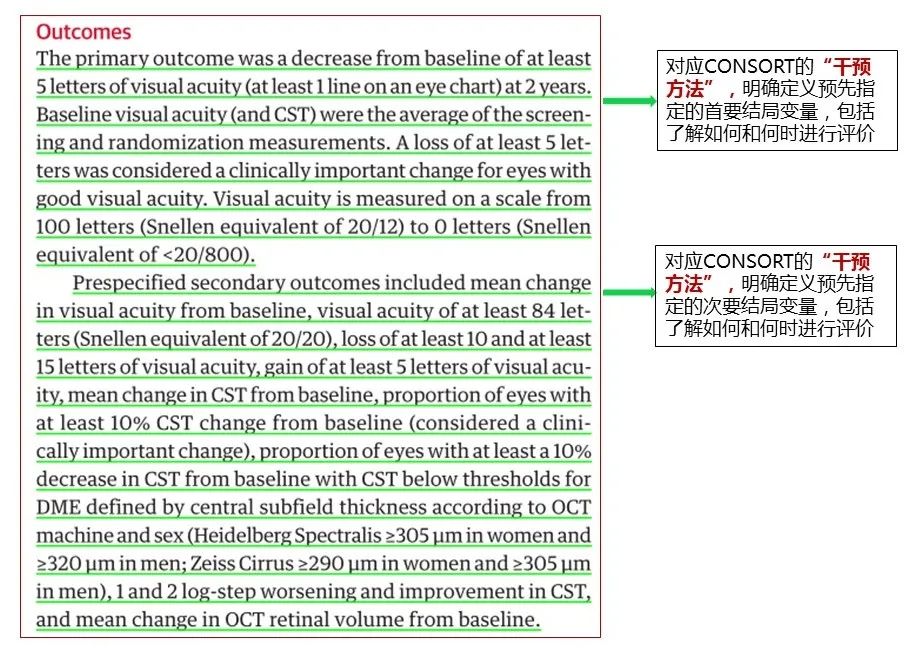
结局指标
6a明确定义预先指定的首要和次要结局变量,包括了解如何
和何时进行评价
6b如果在试验开始后对结局变量进行修改,必须说明原因
样本量大小
7a如何确定样本量
7b必要时,解释期中分析及试验终止原则

随机化
随机序列产生的方法
8a序列产生;分配遮蔽;实施
8b随机化形式,以及描述随机细节(如是否有区组化,有的话,区组是多少?)

遮蔽实施的细节
9 遮蔽的细节
随机实施方法
10随机化序列如何产生,谁招募受试者,谁干预实施
盲法
11a若使用了盲法,需指明谁是干预的被盲者(例如受试者、干预给予者、结果评价者)以及如何设盲
11b如若涉及,描述每组干预的相似性

统计方法
12a用于比较组间主要和次要结局的统计学方法
12b附加分析的统计学方法,比如亚组分析和校正分析



中山眼科中心临床研究中心
获取最新研究资讯
了解最新政策信息
掌握最新机构动态
推送最新受试招募
---来源:临床研究中心---
---供稿:靳光明---
---编辑:郭燕婷---
---审核:陈翔---
---审定:张秀兰---